Pustulosis exantemática generalizada aguda por paracetamol: presentación de un caso
Acute generalized exanthematous pustulosis due to paracetamol: a case report
Alvaro Rojas Mora 1*, https://orcid.org/0000-0001-6805-5364
Aylet Pérez López 1, https://orcid.org/0000-0003-4629-9995
Graciela Fundora Guerra 1, https://orcid.org/0009-0000-9273-0403
1 Hospital Universitario General Calixto García. La Habana, Cuba.
*Autor para correspondencia: alvarorojasmorapiel@gmail.com
Recibido: 03/01/2026
Aceptado: 22/02/2026
Cómo citar este artículo: Rojas-Mora A; Pérez-López A; Fundora-Guerra G. Pustulosis exantemática generalizada aguda por paracetamol: presentación de un caso. MedEst. [Internet]. 2026 [citado acceso fecha]; 6:e475. Disponible en: https://revmedest.sld.cu/index.php/medest/article/view/475
RESUMEN
Introducción: La Pustulosis Exantemática Generalizada Aguda, es una reacción adversa cutánea grave e infrecuente y principalmente inducida por fármacos, clasificada dentro de las reacciones cutáneas adversas graves. Se caracteriza por la aparición súbita de pústulas no foliculares, estériles, sobre una base eritematosa y edematosa, acompañado de fiebre y leucocitosis con neutrofilia.
Objetivo: Reportar un caso típico de Pustulosis Exantemática Generalizada Aguda por paracetamol, confirmado mediante criterios diagnósticos estandarizados.
Presentación del caso: Presentamos el caso de un paciente masculino de 24 años con Pustulosis Exantemática Generalizada Aguda desencadenada por paracetamol. El cuadro clínico típico de fiebre y pústulas no foliculares sobre base eritematosa junto con la histopatología compatible y una puntuación de 11 puntos en la escala por el Estudio Europeo de Reacciones Cutáneas Adversas Graves, confirmaron el diagnóstico. El manejo se basó en la suspensión inmediata del fármaco y corticoides sistémicos, con resolución completa en 3 semanas.
Conclusiones: Este caso ejemplifica que el paracetamol, un medicamento de uso común, puede inducir reacciones cutáneas graves. Demuestra la utilidad de las escalas validadas para un diagnóstico preciso. Reafirma la importancia de una anamnesis farmacológica exhaustiva en dermatología. El desenlace favorable subraya que el pilar del tratamiento es la identificación y retirada del agente causal.
Palabras Clave: Pustulosis Exantemática Generalizada Aguda; Paracetamol.
ABSTRACT
Introduction: Acute Generalized Exanthematous Pustulosis is a rare and severe cutaneous adverse reaction, primarily induced by drugs, and classified as a severe cutaneous adverse reaction. It is characterized by the sudden appearance of non-follicular, sterile pustules on an erythematous and edematous base, accompanied by fever and leukocytosis with neutrophilia.
Objective: To report a typical case of Acute Generalized Exanthematous Pustulosis due to paracetamol, confirmed using standardized diagnostic criteria.
Case presentation: We present the case of a 24-year-old male patient with Acute Generalized Exanthematous Pustulosis triggered by paracetamol. The typical clinical presentation of fever and non-follicular pustules on an erythematous base, along with compatible histopathology and a score of 11 on the European Study of Severe Cutaneous Adverse Reactions scale, confirmed the diagnosis. Management consisted of immediate discontinuation of the drug and systemic corticosteroids, with complete resolution within 3 weeks.
Conclusions: This case exemplifies that paracetamol, a commonly used medication, can induce severe skin reactions. It demonstrates the usefulness of validated scoring systems for accurate diagnosis. It reaffirms the importance of a thorough drug history in dermatology. The favorable outcome underscores that the cornerstone of treatment is the identification and withdrawal of the causative agent.
Keywords: Acute Generalized Exanthematous Pustulosis; Paracetamol.
INTRODUCCIÓN
La Pustulosis Exantemática Generalizada Aguda (PEGA, AGEP por sus siglas en inglés) constituye una reacción cutánea adversa grave (RCASG) infrecuente, con una incidencia estimada de 1-5 casos por millón de personas-año. (1) Aproximadamente el 90 % de los casos están inducidos por fármacos, siendo los antibióticos betalactámicos, quinolonas y sulfonamidas los agentes más frecuentemente implicados. (2,3)
Clínicamente se caracteriza por el inicio abrupto de fiebre alta (>38°C) y erupción generalizada compuesta por pústulas no foliculares, estériles y subcórneas, sobre base eritematosa y edematosa, típicamente iniciándose en pliegues cutáneos y diseminándose al tronco y extremidades, con respeto característico de palmas y plantas. (1)
La leucocitosis con neutrofilia es frecuente, y el compromiso mucoso, cuando presente, suele ser leve. (2) La confirmación diagnóstica se fundamenta en la correlación clínico-patológica, apoyada por la escala validada del grupo EuroSCAR, que otorga 8-12 puntos para casos definitivos. (4)
Aunque el paracetamol (acetaminofén) es uno de los analgésicos más utilizados mundialmente y generalmente considerado seguro, (5) su capacidad para inducir reacciones de hipersensibilidad graves, incluyendo PEGA, está documentada pero permanece subreconocida en la práctica clínica. (6) Esta entidad es particularmente relevante dado el perfil de seguridad atribuido al fármaco y su disponibilidad sin prescripción médica en múltiples países, lo que puede retrasar la identificación del agente causal y perpetuar la exposición al fármaco desencadenante
A pesar de ser una entidad bien caracterizada, su baja incidencia conlleva un reconocimiento clínico insuficiente, lo que puede derivar en diagnósticos erróneos o tardíos. Por ello, el presente trabajo tiene como objetivo: reportar un caso de Pustulosis Exantemática Generalizada Aguda (PEGA) inducida por paracetamol, con el fin de ilustrar su presentación clínica, confirmación diagnóstica mediante criterios estandarizados (escala EuroSCAR) y evolución tras la intervención terapéutica.
PRESENTACIÓN DEL CASO
Paciente masculino de 24 años, previamente sano, sin antecedentes médicos ni alérgicos de relevancia. Consultó al servicio de urgencias por cuadro de 48 horas de evolución caracterizado por fiebre de 39 °C, escalofríos, malestar general y erupción cutánea pruriginosa iniciada en región torácica anterior. Como antecedente farmacológico relevante, refirió el consumo de paracetamol 500 mg cada 8 horas (1,5 g/día) durante 3 días previos, para cefalea tensional. No otros medicamentos, ni síntomas respiratorios, gastrointestinales o urinarios previos. Negó uso de productos tópicos nuevos, metales o viajes recientes.
Examen físico general:
Al ingreso, el paciente se encontraba febril (39°C), hemodinámicamente estable, sin signos de dificultad respiratoria ni afectación del estado general más allá del cuadro descrito.
Examen dermatológico:
Se observaron múltiples pústulas no foliculares, milimétricas, diseminadas sobre una base eritematosa y edematosa en cuello, región anterior y posterior del tórax (Figuras 1 y 2). El eritema era blanqueable a la digitopresión. No se evidenciaron lesiones en mucosas, palmas ni plantas. El resto de la exploración cutánea resultó normal.
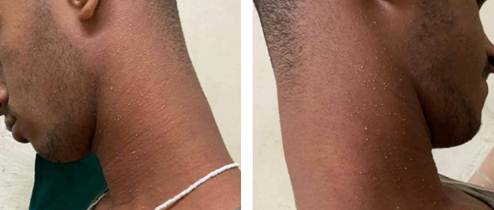
Figura 1: Visión anterolateral del cuello. Se observan múltiples pústulas no foliculares, milimétricas, diseminadas simétricamente sobre una base eritematosa, características de la fase aguda de la Pustulosis Exantemática Generalizada Aguda.
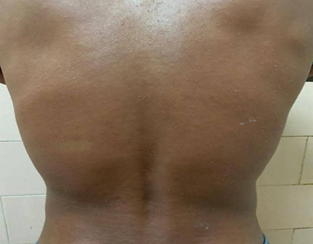
Figura 2: Región posterior del tórax. Se aprecian numerosas pústulas no foliculares, milimétricas, distribuidas de forma difusa sobre una base eritematosa.
Exámenes Complementarios
Los estudios paraclínicos revelaron los siguientes hallazgos:
-Hemograma completo: Leucocitosis (17.4 × 10⁹/L) con neutrofilia marcada (87 %), eosinofilia leve (3 %) y linfocitosis relativa (13 %). Hematocrito: 0.44. Recuento de plaquetas: 220 × 10⁹/L.
-Reactantes de fase aguda: Velocidad de sedimentación globular (VSG): 30 mm/h.
-Función renal: Creatinina sérica: 50 µmol/L (valores dentro de límites normales).
-Función hepática: Transaminasas dentro de rangos normales (TGP: 16 U/L, TGO: 20 U/L).
-Serologías: VIH y serología general no reactivas.
-Biopsia cutánea: El estudio histopatológico mostró una pústula subcórnea con abundantes neutrófilos, espongiosis y exocitosis neutrofílica en la epidermis. En la dermis se observó un infiltrado inflamatorio perivascular mixto, compuesto por neutrófilos y eosinófilos. Estos hallazgos fueron compatibles con una reacción de hipersensibilidad aguda y concordante con el diagnóstico propuesto.
Diagnóstico: Pustulosis Exantemática Generalizada Aguda (PEGA) inducida por paracetamol. Código CIE-11: ED30.1. Puntuación EuroSCAR: 11 puntos (pústulas típicas: 2; eritema típico: 2; distribución típica: 2; fiebre >38 °C: 1; neutrofilia ≥7.000 células/mm³: 1; histología compatible: 3), correspondiente a caso definitivo.
Tratamiento Instaurado
El manejo terapéutico se basó en los siguientes pilares:
1-Suspensión inmediata y permanente del fármaco causal: Se descontinuó por completo la administración de paracetamol.
2-Tratamiento sintomático: Se inició con Difenhidramina 25 mg vía oral cada 8 horas (por 7 días) para el control del prurito.
3-Corticoterapia sistémica: Se indicó prednisona oral a una dosis de 1 mg/kg/día, con el objetivo de modular la respuesta inflamatoria.
4-Cuidados tópicos: Se prescribieron baños emolientes diarios y aplicación tópica de loción de óxido de zinc al 2%, dos veces al día, para proteger la piel y favorecer la cicatrización.
No se realizaron pruebas de parche ni test de provocación controlada por riesgo de reacción recurrente.
Evolución y Seguimiento
El paciente mostró una respuesta clínica favorable. En la reevaluación a los 12 días, se observó una mejoría notable: desaparición completa de las pústulas, marcada reducción del eritema y presencia de una fina descamación residual. Un control posterior a la tercera semana confirmó la resolución completa del cuadro sin evidencia de secuelas cutáneas o sistémicas.
Consentimiento informado: Se obtuvo consentimiento informado escrito del paciente para la publicación de este caso clínico, garantizando la confidencialidad de su identidad mediante la eliminación de datos identificables.
DISCUSIÓN
La Pustulosis Exantemática Generalizada Aguda (PEGA) constituye una dermatosis reactiva infrecuente que, aunque tipificada en 1968, permanece subdiagnosticada en la práctica clínica habitual. (1) El caso presentado ilustra la presentación prototípica de esta entidad: inicio abrupto (<24 horas), fiebre alta, pústulas estériles no foliculares sobre base eritematosa con distribución en tronco y pliegues, leucocitosis con neutrofilia marcada, y evolución favorable tras suspensión del fármaco causal. (2,3)
El diagnóstico de PEGA requiere exclusión de entidades pustulosas sistémicas. En este caso, la ausencia de antecedente psoriásico, la distribución atípica para psoriasis pustulosa (respeto de palmas y plantas), y la latencia corta (3 días) respecto al inicio del paracetamol, descartaron psoriasis pustulosa generalizada. (4) El síndrome de Stevens-Johnson y la necrólisis epidérmica tóxica se excluyeron por ausencia de compromiso mucoso severo, atipia de las lesiones (pústulas vs. máculas/máculopápulas), y evolución rápida favorable. (5) Las infecciones bacterianas (estafilococia, estreptococia) se descartaron por esterilidad de las pústulas, ausencia de signos sistémicos de infección y respuesta inmediata al retiro del fármaco sin antibioterapia. (6)
La confirmación mediante la escala EuroSCAR (11/12 puntos) estableció el diagnóstico con alto nivel de certeza. Esta herramienta validada, desarrollada por el grupo EuroSCAR, ha demostrado especificidad del 98 % y sensibilidad del 80 % para discriminar PEGA de otras RCASG. (6) La puntuación obtenida supera ampliamente el umbral de "caso definitivo" (≥8 puntos), reforzando la validez del reporte.
Aunque los antibióticos betalactámicos concentran el 40-50% de los casos de PEGA farmacodinámica, el paracetamol se identifica como causal en aproximadamente el 3-5 % de los casos según registros europeos. La relevancia de esta asociación radica en el perfil de seguridad atribuido al fármaco y su estatus de venta libre en múltiples países, incluyendo Cuba. (8-10)
La latencia observada (3 días desde el inicio del paracetamol hasta la aparición de síntomas) es característica de las reacciones de hipersensibilidad inmediata mediadas por células T (reacción tipo IVc según clasificación de Gell y Coombs modificada). Este mecanismo inmunológico, distinto de la toxicidad directa por metabolitos hepatotóxicos (N-acetil-p-benzoquinona imina), explica la individualidad de la respuesta y la imposibilidad de predecirla mediante dosis terapéutica. (11) La presentación en primer exposición documentada sugiere sensibilización previa subclínica o reacción heteroalérgica por determinantes antigénicos compartidos. (12,13,14)
La elección de corticoterapia sistémica oral (prednisona 1 mg/kg/día) se fundamentó en la extensión cutánea (>50% superficie corporal) y el malestar sistémico significativo. (15,16) Aunque la PEGA es autolimitada, los corticoides aceleran la resolución en aproximadamente 3-5 días según evidencia observacional⁵. No se indicó corticoterapia intravenosa ni hospitalización prolongada dada la estabilidad hemodinámica, ausencia de compromiso orgánico y cumplimiento familiar adecuado.
La decisión de no realizar pruebas de parche o test de provocación oral controlada se justificó por: (a) diagnóstico clínico-patológico definitivo, (b) riesgo de recurrencia potencialmente severa, y (c) disponibilidad de alternativas analgésicas efectivas. (17) Esta decisión concuerda con recomendaciones de sociedades dermatológicas europeas para casos de certeza diagnóstica alta. (6)
Este caso subraya la necesidad de sistemas de notificación de reacciones adversas a medicamentos de venta libre. El paracetamol, consumido por el 80 % de la población adulta cubana al menos una vez al año, genera falsa seguridad que retrasa el diagnóstico de reacciones graves. La anamnesis farmacológica exhaustiva debe incluir explícitamente "automedicación" y productos considerados "inocuos".(18)
La notificación de este caso al Centro Nacional de Farmacovigilancia contribuye a la caracterización del perfil de seguridad real del paracetamol y refuerza la vigilancia postcomercialización de medicamentos de uso masivo.
CONCLUSIONES
Este caso confirma el diagnóstico de Pustulosis Exantemática Generalizada Aguda (PEGA) inducida por paracetamol, validado por la escala de EuroSCAR, ilustra la capacidad de fármacos de uso común para desencadenar reacciones de hipersensibilidad grave. La evolución favorable tras la suspensión del agente causal y el tratamiento sistémico oportuno reafirma el carácter autolimitado de la entidad. El reporte refuerza la necesidad de una anamnesis farmacológica rigurosa y contribuye a la farmacovigilancia, recordando que ningún medicamento está exento de riesgos adversos graves.
REFERENCIAS BIBLIOGRÁFICAS
1. Saavedra S, Briceño M, Pajuelo G, Sandoval B. Pustulosis exantematosa generalizada aguda. An Fac Med (Lima). 2021;82(4):322-5. DOI:10.15381/anales.v82i4.21025
2. Puebla-Miranda M, González-Rivera C, Reséndiz-Carmona G, Vázquez-Velo JA. Pustulosis exantemática aguda generalizada. Dermatol Rev Mex. [Internet] 2023 [citado 02/01/2026]; 67(4):536-42. Disponible en: https://dermatologiarevistamexicana.org.mx/article/pustulosis-exantematica-aguda-generalizada/
3. Moore MJ, Sathe NC, Ganipisetti VM. Pustulosis exantemática generalizada aguda [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 [citado 02/01/2026]. Disponible en: https://www.ncbi.nlm.nih.gov/books/NBK592407/
4. Sapia E, Lascano F, García Zubillaga P, Dastugue M. Pustulosis exantemática aguda generalizada. Rev Hosp Niños (B Aires). [Internet]. 2019 [citado 02/01/2026]; 61(274):159-64. Disponible en: https://revfdc.sld.cu/index.php/fdc/article/view/190
5. Lizardo-Castro GA, Guillén-Mejía GW. Acute generalized exanthematous pustulosis. Bol Med Hosp Infant Mex. 2022;79(4):268-73. DOI:10.24875/BMHIM.22000268
6. Stadler P, Oschmann A, Kerl K, Maul J, Oppel E, Schiesser B, et al. Acute generalized exanthematous pustulosis: clinical characteristics, pathogenesis, and management. Dermatology. 2023;239:328-33. DOI:10.1159/000529218
7. Alfalah M, Alotaibi Y, Alotaibi A, Alharthi R. Acute generalized exanthematous pustulosis induced by iodinated contrast media: a case report. Dermatol Reports. 2025;17(4):10217. doi:10.4081/dr.2025.10217
8. Tejera Díaz JF, González González L, Hurtado Gascón L, Portela Arrieta MC, Delgado Silva M, Cansino Carvajal L, et al. Pustulosis exantemática generalizada aguda. Folia Dermatol Cubana [Internet]. 2023 [citado 02/01/2026]; 16(1). Disponible en: https://revfdc.sld.cu/index.php/fdc/article/view/307
9. Vallejo-Yagüe E, Martinez-De la Torre A, Mohamad OS, Sabu S, Burden AM. Desencadenantes farmacológicos y cuadro clínico de la pustulosis exantemática aguda generalizada (PEAG): una serie de casos de 297 pacientes. J Clin Med. 2022;11(2):397. DOI:10.3390/jcm11020397
10. Creadore A, Desai S, Alloo A, Dewan AK, Bakhtiar M, Cruz-Diaz C, et al. Clinical Characteristics, Disease Course, and Outcomes of Patients With Acute Generalized Exanthematous Pustulosis in the US. JAMA Dermatol. 2022;158(2):176-183. doi:10.1001/jamadermatol.2021.5390
11. Hadavand MA, Kaffenberger B, Cartron AM, Trinidad JCL. Clinical presentation and management of atypical and recalcitrant acute generalized exanthematous pustulosis. J Am Acad Dermatol. 2022;87(3):632-639. doi:10.1016/j.jaad.2020.09.024
12. de Groot AC. Results of patch testing in acute generalized exanthematous pustulosis (AGEP): A literature review. Contact Dermatitis. 2022;87(2):119-141. doi:10.1111/cod.14075
13. Castanedo-Lara LM, Sánchez-Olivo N. Pustulosis exantemática aguda generalizada inducida por metotrexato. Reacción adversa infrecuente pero potencialmente grave. Dermatol Rev Mex. [Internet]. 2025 [citado 02/01/2026]; 69(6):930-2. Disponible en: https://dermatologiarevistamexicana.org.mx/article/pustulosis-exantematica-aguda-generalizada-inducida-por-metotrexato-reaccion-adversa-infrecuente-pero-potencialmente-grave/
14. Gómez-Chicre V, Camacaro MG, Guijarro J, López de la Torre M, Martínez Díaz N, Abadía L. Pustulosis exantemática generalizada aguda en paciente pediátrico polimedicado con traumatismo craneoencefálico. Rev Asoc Colomb Dermatol. 2022;30(1):52-9. DOI:10.29176/2590843X.1730
15. Parisi R, Shah H, Navarini AA, Serra-Baldrich E, Veraldi S, Rieder F, et al. Acute generalized exanthematous pustulosis: clinical features, differential diagnosis, and management. Am J Clin Dermatol. 2023;24(4):557-75. DOI:10.1007/s40257-023-00779-3
16. Santos MI, Sousa M, Cerqueira P, Ambrioso I, Moniz Ramos M. A case of acute generalized exanthematous pustulosis induced by ceftriaxone. Cureus. 2023;15(3):e36281. DOI:10.7759/cureus.36281
17. Shi D, Ghias M, Haris A, Heubach K. Acute generalized exanthematous pustulosis in a patient with Crohn's disease being treated for streptococcal pharyngitis and sternoclavicular joint abscess. Cureus. 2025;17(1):e77595. DOI:10.7759/cureus.77595
18. Vo VA, Dupuy E, Rukasin CRF. Combination testing confirming clindamycin induced acute generalized exanthematous pustulosis. JAAD Case Rep. 2025;63:77-80. DOI:10.1016/j.jdcr.2025.06.005
CONTRIBUCIÓN DE AUTORÍA
ARM: Conceptualización, investigación, curación de datos, metodología, visualización, redacción del borrador original, así como revisión y edición del manuscrito final.
ALP: Conceptualización, investigación y supervisión.
GFG: Conceptualización, investigación y supervisión.
CONFLICTO DE INTERESES
Los autores declaran no tener conflicto de intereses.
FUENTES DE FINANCIACIÓN
Los autores no recibieron financiación para el desarrollo del artículo.
USO DE INTELIGENCIA ARTIFICIAL
Los autores declaran que no se utilizó inteligencia artificial en la redacción de este manuscrito.